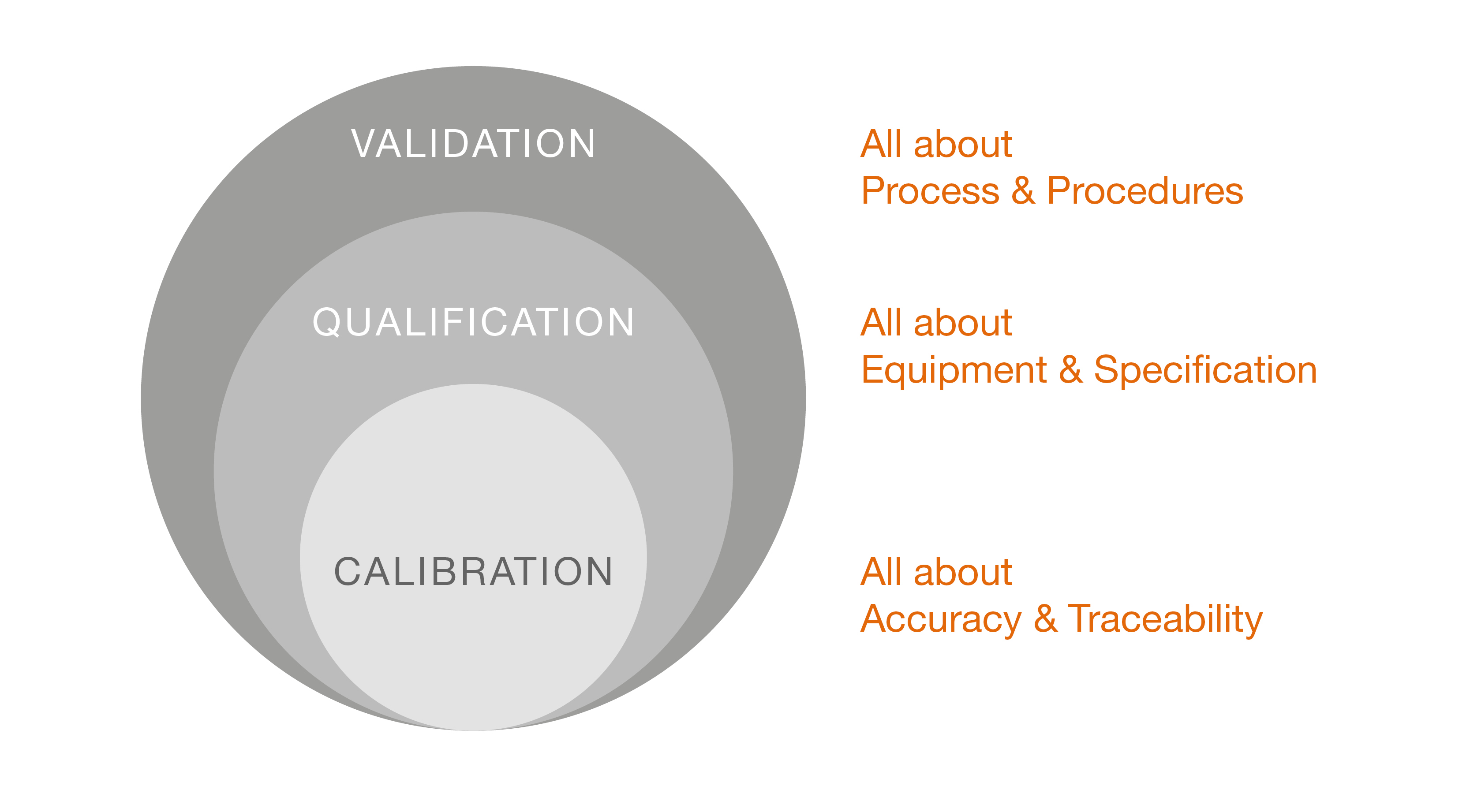
La validation est le processus documenté de vérification qu'un système, un procédé, un équipement ou un produit répond de manière fiable aux exigences spécifiques et aux normes de qualité. Ce procédé garantit que tous les paramètres critiques sont contrôlés et produisent systématiquement des résultats reproductibles afin de garantir à la fois la sécurité et l'efficacité du produit final. Ainsi, la validation est la preuve documentée que toutes les procédures, processus, installations, systèmes, matériaux et équipements respectent les exigences GxP et fournissent les résultats attendus.